Тюрин В.П., Мезенова Т.В., Кирюхина Н.А., Аблицов А.Ю., Орлов С.С., Кулабухов В.В., Антропова Н.В.
Первым термин «Микроскопический узелковый периартериит» использовал F.Wohlwwill в 1922 г. при описании двух пациентов с трансмуральным периартериитом и гломерулонефритом. Оба пациента погибли от болезни, протекавшей с миалгиями, парезом и гломерулонефритом. Ни в одном из случаев не было обнаружено ни макроскопических изменений сосудов, ни аневризм, ни узелков, характерных для классического узелкового периартериита. F.Wohlwwill был убежден, что описанное им заболевание представляет собой форму узелкового периартериита. Он также обнаружил в образцах признаки венулита, но считал, что вовлечение вен, по крайней мере, частично - независимо от артериита. Некоторые авторы еще до F.Wohlwwill (в том числе Оphuls, Beitzke, Walter и von Haun) описывали поражение вен, которое в настоящее время считается более характерным для микроскопического полиангиита, нежели для классического узелкового полиатериита. Микроскопический полиангиит имеет быстропрогрессирующее течение, с развитием осложнений, приводящих к летальному исходу. Причиной смерти обычно являются массивные легочные кровотечения, инфекционные осложнения. Редкость патологии создает дополнительные трудности своевременной диагностики заболевания.
Пациентка Ш, 58 лет, заболела остро в начале декабря 2007 г., когда появились общая слабость, повышение температуры тела до 37-37,5С, заложенность носа, малопродуктивный кашель. Диагностирована ОРВИ, начата терапия ципрофлоксацином 1,0 г/сут, эреспалом. На фоне проводимой терапии сохранялось повышение температуры тела до 38С, потливость. На третьи сутки заболевания выполнена рентгенография органов грудной клетки, выявлена пневмоническая инфильтрация в нижней доле правого легкого. Диагностирована очаговая пневмония, продолжена амбулаторная терапия ципрофлоксацином. Однако, состояние пациентки быстро ухудшалось: нарастала интоксикация, появились кровохарканье, одышка при физической нагрузке, похудание.
Госпитализирована в ЦКБ Гражданской авиации с диагнозом: очаговая пневмония. Анализ крови при поступлении: гемоглобин 82 г/л, лейкоциты 20х109/л, СОЭ 80 мм/час. При КТ грудной клетки 24.12.07 подтвержден диагноз двусторонней полисегментарной пневмонии (рис. 1). Назначен роцефин 2,0 г/сут. Осмотрена фтизиатром, который исключил специфическое поражение легких.
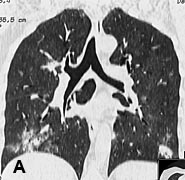 | 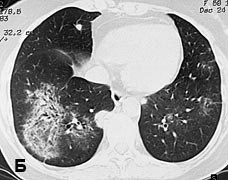 | 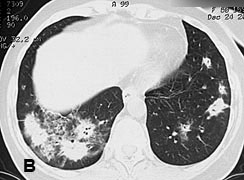 |
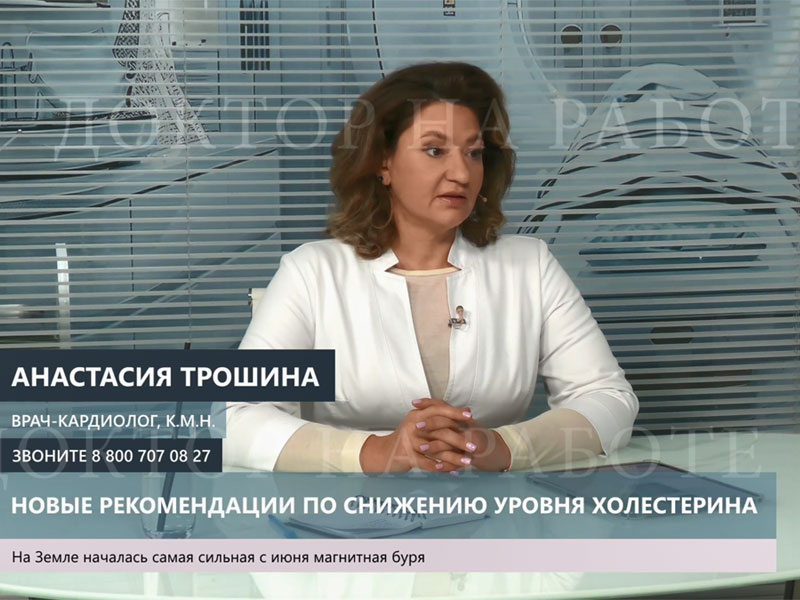
Рис 1. КТ органов грудной клетки с реконструкцией от 24.12.2007: двусторонняя сливная пневмония. Видны зоны инфильтрации легочной ткани.
А – фронтальная плоскость; Б, В – горизонтальная плоскость. Через 2 недели при контрольной рентгенографии легких, а затем при КТ органов грудной клетки от 11.01.08. выявлена отрицательная динамика: тотальная пневмония с элементами деструкции справа, сливная нижнедолевая пневмония слева, реактивный плеврит (рис. 2). С подозрением на тотальную двухстороннюю септическую деструктивную пневмонию 11.01.08 больная была переведена в отделение реанимации центра гнойно-септической хирургии НМХЦ им. Н.И.Пирогова.
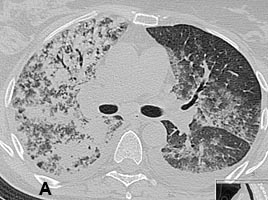 | 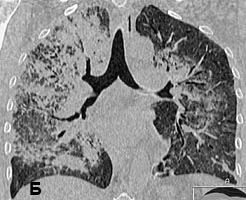 |
Рис 2. КТ органов грудной клетки от 11.01.2008. с реконструкцией: обширная диссеминация мелких «просовидных» теней на фоне диффузной очаговой пневмонии: инфильтрации со склонностью к слиянию; выраженные интерстициальные изменения.
При поступлении состояние тяжелое. Вынужденное положение в кровати с приподнятым головным концом. Температура тела 39,30С. Тахипное до 26-30 в мин. Над всеми отделами легких выслушивались крепитирующие хрипы. Кровохарканье до 80-100 мл. Пульс 118 в мин., ритмичный, удовлетворительного наполнения. Тоны сердца приглушены, АД 140/65 мм рт. ст. Анализ крови от 12.01.08: гемоглобин 80 г/л, лейкоцитоз до 16х109/л, СОЭ 80 мм/час, п – 5%, с – 73%, л - 15%, м - 5%, э – 2%, тромбоциты 460х109/л. АСТ 54 ед/л, АЛТ 46,3 ед/л, билирубин общ. 25,8 мкмоль/л, билирубин пр. 6,1 мкмоль/л, амилаза 118 ед/л, креатинин 91,6 мкмоль/л, белок 63 г/л, альбумин 28 г/л. СРБ – 24 мг/л. Фибриноген 7,88 г/л. Анализ мочи от 12.01.08 – относительная плотность 1013, белок 0.033 г/л, л - 2-4 в п/зр., эр - 17 в п/зр.
У больной заподозрен микроскопический полиангиит. С целью морфологического подтверждения рабочего диагноза через двое суток после поступления в стационар была проведена краевая резекция легкого из миниторакотомного доступа. После этого начата пульс-терапия солумедролом 0.5 г/сутки в течение 4-х дней, однократно циклофосфан 800 мг/сут. в/в капельно. Своеобразная рентгенологическая картина легких в виде обширной диссеминации легких, просовидных теней на фоне диффузной очаговой инфильтрации со склонностью к слиянию и выраженных интрестициальных изменений, развившихся на фоне антибактериальной терапии требовала проведения дифференциальной диагностики между грибковым поражением легких (аспергиллез, криптококкоз), туберкулезом легких, синдромом Гудпасчера.
При обследовании посевы крови на стерильность роста микрофлоры не дали; в мокроте микобактерии туберкулеза, аспергиллы, криптококки не обнаружены. ИФА на антитела к микобактериям туберкулеза отрицательная. Антинейтрофильные цитоплазматические антитела (АНЦА) к протеиназе-3 - 640 (повышены), к миелопироксидазе < 10 и антитела к базальной мембране почек < 10 (в норме). АНЦА являются специфичными антителами к антигенам цитоплазмы, содержащимся в гранулах нейтрофилов, лизосомах моноцитов и в норме не определяются. В активную фазу микроскопического полиангиита АНЦА обнаруживаются практически у 100% больных, поэтому его относят к АНЦА-ассоццированным формам васкулитов мелких сосудов. По данным гистологического исследования биопсии легких альвеолы со склерозированными перегородками, просвет заполнен фибрином, гипертрофия мышечной оболочки артерий, склероз стенок бронхов и артерий (рис 3).
На основании тотального деструктивного поражения легких с длительно сохранявшимся кровохарканьем, поражением почек, повышением титра АНЦА к протеиназе и данных гистологического исследования - у пациентки диагностирован микроскопический полиангиит. Критерии диагностики заболевания у пациентки полностью соответствовали критериям микроскопического васкулита, предложенных Watts R.A., Scott D.S. (2003): инфильтративно-деструктивное поражение легких (у 50% пациентов), поражение почек (у 100% пациентов), антинейтрофильные антитела (в остром периоде - до 100% пациентов), гистологическое подтверждение.
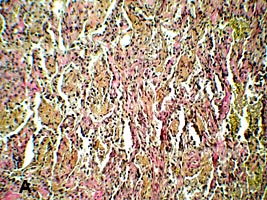 | 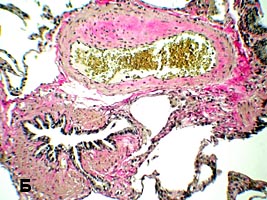 |
Рис 3. Биопсия легкого. Микрофото: А - альвеолы со склерозированными перегородками заполнены фибрином; Б - склероз стенок бронхов и артерий.
На фоне проводимой пульс-терапии солумедролом и циклофосфаном состояние и самочувствие быстро улучшались: температура тела стойко нормализовалась на 2 день, кровохарканье сохранялось еще 4 суток. В дальнейшем проводилась терапия метипредом 40 мг/сут., 2 недели аугментином 2,0 г/сут., противогрибковая терапия вифендом, (до иммунологического подтверждения диагноза). Клинический анализ крови, мочи от 7.02.08 в пределах нормы. В удовлетворительном состоянии 8.02.08 выписана на амбулаторное лечение. В марте 2008 приступила к работе. При контрольной КТ органов грудной клетки в марте 2008: инфильтративных изменений в легких не выявлено (рис 4). Клинический анализ крови в пределах нормы. Жалоб нет. Начато снижение дозы метипреда по схеме, к терапии добавлен метотрексат 10 мг/нед. с гормонсберегающей целью.
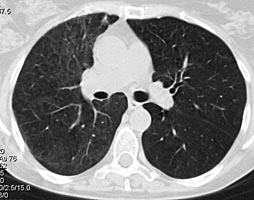 | 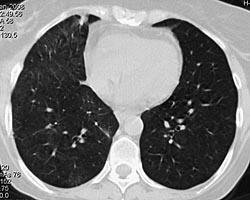 |
Рис 4. КТ органов грудной клетки 18.03. 2008: в легких изменений нет. Особенностью представленного клинического наблюдения явилось деструктивное поражение легких в дебюте заболевания, являющееся проявлением микроскопического полиангиита лишь в 50% случаев. Адекватное, максимально быстрое начало лечения при столь грозном заболевании позволяет достигать ремиссии более чем у 65% пациентов.