Механическая желтуха — этот синдромный диагноз даже в современных условиях развития медицины нередко вызывает у врачей заметное и вполне объяснимое беспокойство. Такие больные требуют проведения не только экстренных диагностических мероприятий в рациональной последовательности и одновременно осмысленной интенсивной терапии, но и срочного выбора правильной тактики лечения.
Желтуха зачастую является первым проявлением различных заболеваний печени, желчевыводящих путей, поджелудочной железы, двенадцатиперстной кишки и др. Как грозное осложнение указанных заболеваний, механическая желтуха (МЖ) значительно утяжеляет состояние пациентов развитием печеночной и почечной недостаточности, кровотечений, гнойных процессов в желчных протоках и печени, а также ряда других осложнений и часто приводит к полиорганной недостаточности.
В последние десятилетия в лечебно-диагностических алгоритмах, используемых при синдроме механической (обтурационной) желтухи в качестве общепринятого стандарта, применяются минимально инвазивные технологии (МИТ). Ведущие клиники, активно занимающиеся этой сложной патологией, как у нас, так и за рубежом, располагают опытом сотен, а то и тысяч подобных наблюдений, позволяющих осуществлять корректный сравнительный анализ используемых технологий в полном соответствии с современными требованиями доказательной медицины.
История
У истоков внедрения и изучения миниинвазивных диагностических и лечебных технологий при синдроме МЖ стояли видные отечественные ученые Б.Петровский, А.Вишневский, В.Виноградов, В.Савельев, А.Шалимов, В.Вишневский, Э.Гальперин, Б.Альперович. Более 30 лет назад на базе клиники факультетской хирургии им. Н.Н.Бурденко
Status quo
Разработка двухэтапного подхода к лечению пациентов с синдромом механической желтухи, а именно — первый этап в зависимости от характера механической желтухи — чрескожные (наружное, наружно-внутреннее желчеотведение, холецистостомия) или эндоскопические методы декомпрессии (эндоскопическая папиллосфинктеротомия, назобилиарное дренирование, билиарное стентирование), второй этап — при возможности традиционное оперативное лечение, при нерезектабельности и неоперабельности — любой вариант установки постоянного стента с применением МИТ, позволили снизить летальность в этой группе пациентов в несколько раз. При этом основная цель стартовых минимально инвазивных вмешательств — улучшить состояние пациента (снизить интоксикацию, желчную гипертензию и гипербилирубинемию, купировать явления холангита и проявления системной воспалительной реакции, предотвратить развитие полиорганной недостаточности и т.п.) и подготовить пациента к основному этапу — оперативному лечению, а значит, и к радикальному устранению причины МЖ. Лишь в ряде случаев при опухолевом генезе механической желтухи и нерезектабельности опухоли различные варианты наружного и внутреннего желчеотведения выходят на первый план и становятся окончательным вариантом лечения. В настоящее время подобный подход к лечению этой тяжелой категории больных с небольшими нюансами принят практически во всех онкологических и хирургических стационарах, а число хирургов, рискующих оперировать на пике механической желтухи, становится всё меньше и меньше, и это, несомненно, отрадный факт.
Основными критериями перехода от одного этапа к другому являются: общее состояние пациента, количество отделяемой желчи и динамика билирубинемии, спектр микробного обсеменения желчи, наличие гнойных осложнений (холангит, холангиогенные абсцессы печени), функциональное состояние печени и другие проявления ПОН. Все критерии анализируются комплексно, при этом малооправданно только на основании оценки одного из них принимать решение о возможности выполнения следующего этапа. Конечно, в практической работе наиболее часто учитываются только биохимические показатели функционального состояния печени, а в некоторых случаях — лишь уровень общего билирубина. При этом известно, что выполнение следующего этапа (операция, стентирование) при уровне общего билирубина более 100 мкмоль/л приводит к таким же грозным осложнениям, как и при уровне
К сожалению, некоторые молодые и, несомненно, талантливые специалисты, начинающие заниматься сложной проблемой МЖ, не всегда начинают свою клиническую практику с изучения и осмысления накопленного опыта (и в первую очередь отечественного). Для того чтобы установить дренаж или стент в желчные протоки, действительно требуется высокая квалификация и профессиональные знания врача, но еще больше мастерства и осмысленных действий требуется для того, чтобы достаточно быстро и квалифицированно оценить состояние больного, наметить правильный дифференциально-диагностический алгоритм и одновременно назначить и провести интенсивную терапию, что особенно важно, вовремя принимать правильные решения при изменении клинической ситуации.
Еще раз подчеркнем, что МЖ — лишь грозное, порой смертельное, осложнение ряда доброкачественных и злокачественных заболеваний, которое следует на первом этапе попытаться разрешить антеградным или ретроградным способом желчеотведения (см. «Руководство по хирургии желчных путей» под ред. Э.И.Гальперина, П.С.Ветшева, 2006, 2009).
Вопрос о преимуществах антеградного или ретроградного способа желчеотведения при различных уровнях «блока» желчных протоков, наверное, самый обсуждаемый. Хотя, казалось бы, всё очевидно, и в клиниках, владеющих всеми современными технологиями (ультразвуковыми, рентгенологическими, эндоскопическими и пр.), такой дилеммы обычно не возникает. Обилие противоречивых мнений и своеобразный статистический «хаос» обусловлены в основном многочисленными сообщениями авторов, владеющих преимущественно одним способом и настойчиво отстаивающих его якобы первостепенное значение в ликвидации МЖ. По понятным причинам такие работы трудно признать корректными и полностью соответствующими современным принципам доказательной медицины, тем более если опыт авторов невелик. Но они, к сожалению, нередко уводят неискушенного специалиста в сторону от принятия оптимального решения в той или иной клинической ситуации.
Выдвинутое ранее аргументированное предложение о том, что МЖ, обусловленную дистальным и средним «блоком», более предпочтительно разрешать эндоскопическими методами, а высокий «блок» — чрескожными методами под контролем УЗИ — (чаще) и КТ-навигацией, является не догмой, но руководством к действию. В то же время клиническая практика свидетельствует, что во многих случаях выбор метода зависит, к сожалению, не только от принципиальных подходов в данной клинической ситуации, но и от уровня развития той или иной службы и квалификации специалистов в конкретном лечебном учреждении, о чем упомянуто выше. Есть примеры, когда при высокой квалификации эндоскопист выполняет желчеотведение и стентирование при «высоких» блоках, за счет мастерства, совершенствования МИТ и применения инструментария последнего поколения, и наоборот, путем чрескожных МИТ удается ликвидировать «низкий» блок. При равноценном и высоком уровне развития эндоскопической, ультразвуковой, рентгенологической службы удается решать сложные клинические проблемы, возникающие при синдроме МЖ, оптимальным образом с учетом накопленного опыта и разработанных алгоритмов. Причем, и это важно, решение принимается коллегиально и сбалансированно с участием мнения специалистов вышеперечисленных служб. Более того, следует отметить важную тенденцию — чем выше квалификация специалистов в эндоскопическом и рентгенохирургическом отделениях, тем чаще возникает потребность в выполнении сочетанных (тандемных, рандеву) операций в наиболее сложных и, казалось бы, неразрешимых в рамках МИТ клинических случаях.
В качестве примера хотелось бы привести одну из них. Пациентка 46 лет, из анамнеза известно, что в феврале 2011 г. ей выполнена операция холецистэктомии с холедохолитотомией. Примерно через месяц после операции сначала появились распирающие боли в верхней половине живота, а затем эпизоды повышения температуры тела, сопровождающиеся ознобом, после возникновения которых стало отмечаться появление желтушного окрашивания склер. При обследовании — явления МЖ, функция печени не нарушена, лейкоцитоз, повышение СОЭ, причиной желтухи, по данным УЗИ и МР-холангиографии, являлись конкременты в левом долевом протоке, самый крупный из которых — диаметром до 1,5 см. По данным ЭРХПГ, внутрипеченочные желчные протоки правой доли печени не изменены, так же как и внепеченочные желчные протоки. Контрастирования желчных протоков левой доли печени не получено (синдром отключенной доли). Попытки эндоскопического удаления конкрементов из левого долевого протока были безуспешными и приводили лишь к миграции в сегментарные протоки с последующим обострением холангита. Пациентка с клинической картиной МЖ и холангита была госпитализирована в НМХЦ им. Н.И. Пирогова в апреле 2011 г.
Понятно, что, исходя из принципов лечения пациентов с механической желтухой и с холангитом, первым этапом следовало выполнить адекватную декомпрессию желчевыводящих путей. Но обстоятельства, то есть индивидуальные особенности пациентки и прежние попытки специалистов другого медицинского учреждения, оставляли мало шансов на успешное применение эндоскопического ретроградного способа. Поэтому было принято коллегиальное решение о целесообразности наружного дренирования желчных протоков левой доли печени под ультразвуковым и рентгенологическим контролем, что и было выполнено.
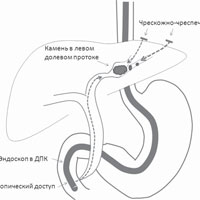
При этом установлено, что причиной формирования конкрементов в желчных протоках левой доли печени является посттравматическая стриктура устья левого долевого протока. При этом наиболее крупный конкремент играл роль клапана, перекрывая ток желчи в области стриктуры, а второй более мелкий конкремент был фиксирован в устье желчного протока второго сегмента печени, также затрудняя отток желчи. Бактериологическое исследование желчи выявило рост патогенной микрофлоры, определена ее чувствительность к антибиотикам. На фоне проводимой комплексной системной и местной терапии удалось справиться с явлениями холангита, снизить интоксикацию, добиться нормализации биохимических показателей. Следующим этапом необходимо было решить вопрос о способе удаления конкрементов из желчных протоков левой доли печени, оставаясь при этом в рамках МИТ. Вариант открытой операции с гепатиколитотомией рассматривался во вторую очередь (как запасной). Отдельно, ни антеградно, ни ретроградно справиться с этой ситуацией было бы невозможно, учитывая расположение конкрементов, анатомические особенности хода желчных протоков. Было принято решение о выполнении сочетанной операции, так называемой технологии рандеву (rendezvous). Первоначально из отдельного доступа выполнено чрескожное наружное дренирование желчного протока второго сегмента печени. Затем через ранее установленный дренаж выполнена дефиксация крупного конкремента в устье левого долевого протока, что позволило ретроградно через эндоскоп завести в левый долевой проток инструмент для удаления конкремента (Рис. 1).
Фиксируя камень чреспеченочно, не позволяя ему мигрировать в проксимальные отделы желчных протоков, нам удалось сначала его фрагментировать, а затем удалить из устья левого долевого протока. Аналогичным образом удалось удалить мелкие конкременты из левого долевого протока, а с помощью второго дренажа — и из устья желчного протока второго сегмента печени. Операция закончена баллонной дилатацией стриктуры левого долевого протока и оставлением наружного страховочного дренажа в левом долевом протоке. На фоне продолжающейся противовоспалительной терапии, через 5 суток после рентгенологического контроля и подтверждения факта адекватной проходимости зоны стриктуры, страховочный дренаж был удален. При динамическом контроле в течение 14 месяцев признаков желчной гипертензии, формирования конкрементов в левом долевом желчном протоке не отмечено.
Подобные операции применяются нами и при опухолевых стриктурах желчных протоков с целью контроля установки стента и профилактики возможных осложнений, коррекции его положения при миграции, реканализации окклюзированного стента или рестентирования.
Quo vadis
Сложность и актуальность проблемы механической желтухи несомненны. Пути улучшения результата лечения этой тяжелой категории больных идут в направлении дальнейшей модификации оборудования, появления новых материалов из нитинола, а значит, и более совершенных инструментов, растет мастерство хирургов, разрабатываются новые сложные операции, накапливается совокупный клинический опыт, появляются молодые целеустремленные врачи, занимающие ся этой многотрудной проблемой, но основные принципиальные подходы к ведению этой сложной категории больных сохраняются.
В последние годы МИТ, хорошо зарекомендовавшие себя в конце прошлого века в качестве диагностических, перешли в разряд лечебно-диагностических. Сейчас трудно себе представить лечебное учреждение без специалистов по эндоскопии и ультразвуковой диагностике, а крупные центры — без оперативной эндоскопии и специализированных отделений рентгенохирургии.
Всё чаще и чаще появляются сообщения о высокой эффективности сочетанного применения МИТ. Но это обстоятельства, хотя и важные (способы, приемы, инновационные технологии, инструменты и т.п.), призванные оптимизировать соблюдение и реализацию основных принципов. По-видимому, здесь уместно будет напомнить известную мудрость: «Обстоятельства переменчивы, принципы — никогда».
Заключение
Эта публикация на страницах весьма авторитетного и популярного медицинского издания, основанная на критическом анализе собственного многолетнего опыта, возможно, окажется полезной коллегам, активно использующим инновационные МИТ, поможет начинающим специалистам в решении сложных диагностических и лечебных вопросов, неизбежно возникающих в лечении этой тяжелой категории больных. По нашему мнению, одной из основных причин существующего трудного положения с диагностикой и лечением больных с МЖ является разобщенность специалистов минимально инвазивной хирургии, отсутствие общества или ассоциации, которые позволили бы постоянно обмениваться опытом, вывести единую точку зрения и определить тактику по многим сложным вопросам. Вероятно, первым шагом в решении этой проблемы может стать научно-практическая конференция с международным участием «Сочетанное применение инновационных минимально инвазивных технологий в многопрофильном стационаре», которая состоится в Национальном медико-хирургическом центре им. Н.И. Пирогова 8 ноября 2012 г. (подробности на сайте www.pirogov-center.ru).
Олег КАРПОВ, профессор
Пётр ВЕТШЕВ, профессор
Сергей БРУСЛИК, доцент
Аяс МААДЫ, доцент
Национальный медико-хирургический центр им. Н.И. Пирогова