Тюрин В.П., Мезенова Т.В., Кирюхина Н.А.
Национальный медико-хирургический центр им. Н.И. Пирогова, Москва
J. Churg, L. Strauss (1951) дали подробное описание 13 наблюдений больных, имевших сочетание тяжелой бронхиальной астмы с гиперэозинофилией и поражением других органов. В 9 из 10 аутопсий авторы отметили воспалительные изменения, свойственные узелковому периартерииту (окклюзии артерий во многих органах), а также участки гранулематозного поражения с эозинофильной инфильтрацией и фибриноидным поражением соединительной ткани и сосудов. Авторы трактовали эту тяжелую патологию с неблагоприятным прогнозом, как злокачественный ангиит. В современных классификациях синдром, описанный Churg, Strauss и названный их именами, рассматривается, как аллергический ангиит. Распространенность синдрома Сhurg-Strauss составляет 1-3 случая на 1 000 000 населения [1]. В литературе представлены противоречивые данные о частоте заболевания мужчин и женщин: соотношение колеблется от 3:1 до 1:2 [2, 3]. В связи с полиморфизмом клинической картины болезни пациенты зачастую первоначально обращаются за медицинской помощью не к ревматологам, а к представителям других специальностей. Редкость патологии создает дополнительные трудности своевременной диагностики заболевания. Примером сложности диагностики может служить следующее наблюдение.
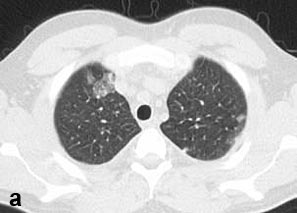
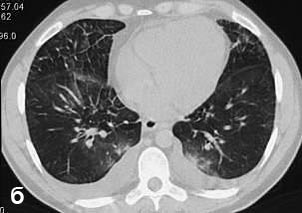
Больной С., 33 г., по профессии электромонтажник, поступил в НМХЦ им. Н.И. Пирогова 5 февраля 2007 г. с жалобами на одышку при незначительной физической нагрузке, кашель с трудноотделяемой мокротой слизистого характера, общую слабость, похудание на 10 кг, субфебрильную температуру тела. С 2000 г. у пациента диагностировали хронический ринит, синусит, полипоз носа. Для купирования затрудненного носового дыхания последние 3 года применял кортикостероидный назальный спрей. В связи с возникновением приступов удушья 2006 г. в НИИ аллергологии и иммунологии диагностирована бронхиальная астма среднетяжелого течения. Назначена терапия симбикортом с положительным эффектом. Ухудшение состояния с декабря 2006, когда появились субфебрильная температура тела, приступы затрудненного дыхания, одышка при физической нагрузке, снижение аппетита. При КТ органов грудной клетки, выполненной амбулаторно 25.01.07г.: лимфаденопатия средостения (лимфоузлы до 2-2,5 см) с образованием конгломерата размером 38 х 40 х 50 мм (рис. 1), снижение прозрачности легочной ткани по типу «матового стекла» (рис. 2а), диффузное уплотнение интерстициальной ткани (рис. 2б), двусторонний гидроторакс. Заподозрена опухоль переднего средостения в связи, с чем пациент госпитализирован для морфологической верификации диагноза.
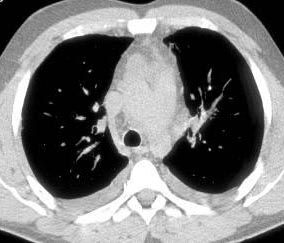 | 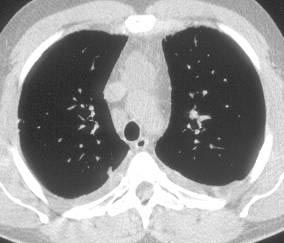 |
| Рис. 1. КТ грудной клетки:
а - в области вилочковой железы образование размером 38х40х50мм, б - увеличение лимфатических узлов средостения до 20-25 мм. | |
 |  |
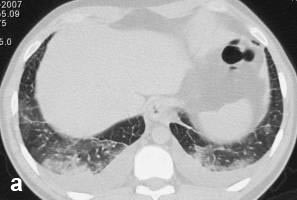 | 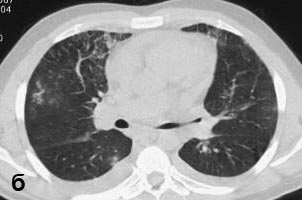 |
| Рис. 2. КТ грудной клетки:
а - снижение прозрачности по типу “матового стекла“, б - диффузное уплотнение интерстициальной ткани. | |
При поступлении состояние тяжелое: вынужденное положение в кровати с приподнятым головным концом, тахипное до 26-30 в минуту. Большую часть ночи спал сидя. При аускультации над легкими дыхание с жестким оттенком, рассеянные разнотональных сухие хрипы на выдохе. Тоны сердца приглушены, ритм галопа, тахикардия до 130-150 в минуту. АД 110/70 мм.рт.ст. Нижний край печени выступал на 4 см. из-под края реберной дуги. Мелкоточечная геморрагическая сыпь на голенях и стопах, фиолетовые пятна неправильной формы по типу «ливедо» в области лодыжек. Температура тела 38-39оС без ознобов и пота. В анализе крови от 05.02.07: лейкоциты 20,4х109/л, гемоглобин 148 г/л, эритроциты 4,9 х 1012/л, э-50%, п-2%, с-35%, л-6%, м-7%, СОЭ-80 мм/ч, АСТ- 29ед/л, АЛТ-100 ед/л, билирубин 13,6 мкмоль/л, глюкоза 4,7 ммоль/л, креатинин 77,9 ммоль/л. Т-тропонин-0,1 нг/мл. Анализ мочи без патологии. На ЭКГ от 05.02.07: синусовая тахикардия, зубцы QS в V1-V3 отведениях, отрицательные зубцы Т в отв. I, AVL, V4-V6 (рис. 3). Изменения ЭКГ позволяли предполагать развитие передне-перегородочного инфаркта миокарда. Однако ЭхоКГ не выявила очагов локального нарушения сократимости стенок левого желудочка. Установлено снижение ФВ до 30% за счет диффузной гипокинезии левого желудочка, увеличение размеров левых предсердия и желудочка (КДР-5,8 см.), повышение систолического давления в легочной артерии до 50 мм. рт. ст.
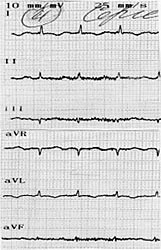 | 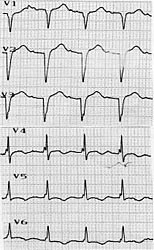 |
| Рис. 3. на ЭКГ зубцы QS отведениях V1-V3. | |
Рентгенография грудной клетки 11.02.07: усиление легочного рисунка с преобладанием застойных изменений с обеих сторон, жидкость в задних синусах, корни расширены, сердце увеличено за счет левого желудочка. При исследовании плевральной жидкости уд. вес 1010, цвет желтый, белок 18 г/л, р. Ривальта слабо положительная, эозинофилия до 77%. Учитывая выраженную эозинофилию дифференциальная диагностика проводилась между гиперэозинофильным синдромом Леффлера и системным некротизирующим васкулитом Чарга-Стросса. С целью уточнения диагноза выполнена биопсия кожно-мышечного лоскута: периваскулярные инфильтраты с большим количеством эозинофилов, поражением артериол с некрозом стенок (рис. 4), картина продуктивного воспаления (рис. 5). При исследовании антинейтрофильных цитоплазматических антител получен отрицательный результат.
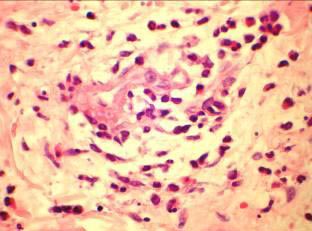
Рис. 4. Поражение артрериол с некрозом стенки | 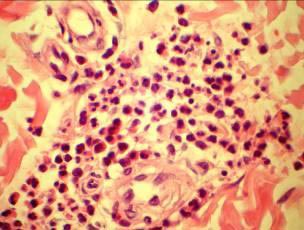
Рис. 5. продуктивное воспаление сосуда, очаговая клеточная инфильтрация эозинофилами |
Анамнестические указания на аллергический риносинусит, полипоз носа, а в последующем и бронхиальную астму, поражение легких (диффузное уплотнение интерстициальной ткани и снижение прозрачности по типу “мaтового стекла” по данным КТ), сердца (диффузные изменения миокарда левого желудочка со снижением сократительной способности миокарда без четких признаков очагово-рубцовых изменений), кожи по типу сосудистой пурпуры и ливедо, гиперэозинофилии периферической крови и плеврального выпота, гистологических признаков продуктивно-некротического васкулита с эозинофильной инфильтрацией кожи и мышц позволили диагностировать системный гранулематозный васкулит – синдром Чарга-Стросса. После проведения биопсии в связи с тяжестью состояния больного назначена терапия солумедролом 250 мг в/в. После гистологического подтверждения диагноза проводилась комбинированная иммуносупрессивная терапия метипредом 40 мг в день внутрь и азатиоприном 100 мг в день. Температура стойко нормализовалась на третий день комбинированной терапии.
В течение недели прошла одышка, уменьшилась тахикардия, над легкими перестали выслушиваться хрипы, подверглись обратному развитию проявления геморрагического васкулита и ливедо. Однократно проведена плевральная пункция с удалением 700 мл выпота соломенно-желтого цвета. При контрольной КТ органов грудной клетки через неделю лечения лимфаденопатия средостения и изменения легочной ткани по типу “мaтового стекла” не определялись (рис. 6). В стационаре прибавил в весе 5 кг. Клинический анализ крови нормализовался с марта 2007 г.
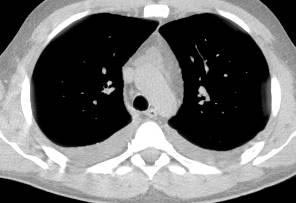 | 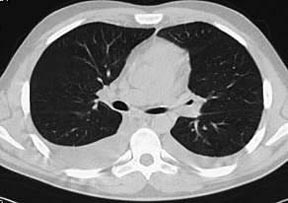 |
| Рис. 6. КТ через месяц лечения: отсутствуют изменения в средостении и легочной ткани | |
После выписки из стационара самочувствие удовлетворительное, в апреле приступил к работе. В мае 2007 доза метипреда снижена до 24 мг/сут, азатиоприн продолжал принимать в прежней дозе. В июне 2007 г. определялись умереннные проявления сердечной недостаточности: легкая пастозность голеней, тахикардия. На ЭКГ и ЭхоКГ сохранялись прежние изменения. К лечению добавлен бисопролол. Особенностью данного клинического наблюдения явилось увеличение лимфатических узлов средостения в дебюте, являющееся редким проявлением синдрома Чарг-Стросса, и направившее диагностический поиск по ложному пути. Наличие конгломерата узлов в проекции вилочковой железы у пациента с субфебрильной температурой тела требовал проведения дифференциальной диагностики с лимфопролиферативными заболеваниями и злокачественной опухолью. Однако полисиндромность поражения в сочетании с большой эозинофилией крови позволили усомниться в опухолевой природе болезни и заподозрить системный васкулит, доказанный в последующем. На фоне комбинированной терапии лимфоаденопатия средостения быстро подверглась обратному развитию. В клинической картине заболевания превалировали проявления нарастающей сердечной и дыхательной недостаточности.
По данным Центра васкулитов Джона Хопкинса наиболее грозными висцеральными проявлениями являются быстроразвивающаяся сердечная недостаточность (наблюдавшаяся у нашего пациента), приводящая в 50-80% случаев к летальному исходу несмотря на активную кортикостероидную терапию; инфаркт миокарда вследствие коронариита; геморрагический или ишемический инсульт в 3-7% случаев вследствие церебрального васкулита; поражение желудочно-кишечного тракта с образованием язв желудка, кишечника, кровотечением, перфорацией язв, перитонитом – в 37-62% случаях. В нашем наблюдении отсутствовало поражение почек, нервной системы и желудочно-кишечного тракта, являющееся типичным проявлениям болезни. Антинейтрофильные цитоплазматические антитела не были повышены. При синдроме Чарга-Стросса они выявляются в 67-80% случаев, реже чем при гранулематозе Вегенера, микроскопическом полиартериите [4]. Поражение сердца, легочные инфильтраты и плеврит чаще наблюдаются у пациентов с отсутствием антител к цитоплазме нейтрофилов, что мы и констатировали у нашего больного. Своевременная диагностика, адекватное, максимально быстрое начало лечения позволяют достигать ремиссии при столь грозном заболевании более чем у 80% пациентов. Развитие хронической сердечной недостаточности требует проведения дополнительной терапии в соответствии с рекомендациями Европейского общества кардиологов (2005).
Литература
- Watts R.A., Carruthers D.M., Scott D.G. Epidemiology of systemic vasculitis: changing incidence of definition? // Semin arthritis rheum. – 1995. – Vol. 25. – P. 28-34.
- Насонов Е.Л., Баранов А.А., Шилкина Н.П. Васкулиты и васкулопатии. Ярославль, 1999, 616 с.
- Семенкова Е.Н. Системные некротизирующие васкулиты. М., Русский врач, 2001, 96 с.
- Вест С.Д. Секреты ревматологии. М., БИНОМ, 2001, 768 с.